Для поліпшення роботи сайту ми використовуємо файли cookie. Продовжуючи переглядати сайт, ви погоджуєтеся з цим.
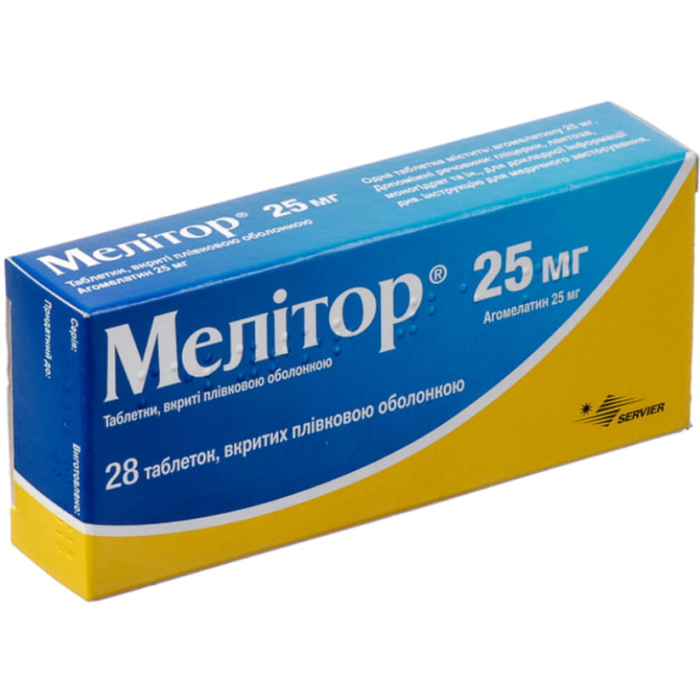
Мелітор 25 мг таблетки №28
618,60 ₴
Servier (Франція)
Арт.
120904

У список
Мелітор 25 мг таблетки №28
Servier (Франція)
Увага! Ціни дійсні тільки при покупці онлайн
Ваше місто - Київ?
Ваше місто
Ірпінь
Товар відсутній в аптеках обраного міста

Самовивіз
Безкоштовно

Кур'єром
Доставка до 48 годин
Безкоштовно від 2000 грн
Рецептурний препарат. Можливий тільки самовивіз з аптеки

Нова Пошта відділення
Доставка від 1 дня
Від 80 грн

Нова Пошта поштомат
Доставка від 1 дня
Від 80 грн

Нова Пошта курʼєр
Доставка від 1 дня
Від 150 грн

Укрпошта відділення
Доставка від 2 днів
Від 52 грн
На сайті
При отриманні
-

 Значення "Можна" вказує на те, що вибраний препарат має мінімальний ризик для здоров'я дорослого населення і результат, очікуваний від вживання лікарського засобу, переважає над можливими ризиками. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем.
Значення "Можна" вказує на те, що вибраний препарат має мінімальний ризик для здоров'я дорослого населення і результат, очікуваний від вживання лікарського засобу, переважає над можливими ризиками. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем. -


-
 Значення "З обережністю" вказує на те, що вибраний препарат може надавати підвищений негативний вплив на здоров'я вагітних жінок, такі лікарські засоби рекомендується вживати, якщо очікуваний результат від застосування цього лікарського препарату переважає над всілякіими ризиками. Щоб уникнути несприятливих наслідків, будь-який медикаментозний препарат слід вживати після консультації з провідним фахівцем.
Значення "З обережністю" вказує на те, що вибраний препарат може надавати підвищений негативний вплив на здоров'я вагітних жінок, такі лікарські засоби рекомендується вживати, якщо очікуваний результат від застосування цього лікарського препарату переважає над всілякіими ризиками. Щоб уникнути несприятливих наслідків, будь-який медикаментозний препарат слід вживати після консультації з провідним фахівцем. -
 Значення "З обережністю" вказує на те, що вибраний препарат може чинити підвищений негативний вплив на здоров'я годуючих жінок, такі лікарські засоби рекомендується вживати, якщо очікуваний результат від застосування даного лікарського препарату переважає над всілякими ризиками. Щоб уникнути несприятливих наслідків, будь-який медикаментозний препарат слід вживати після консультації з провідним фахівцем.
Значення "З обережністю" вказує на те, що вибраний препарат може чинити підвищений негативний вплив на здоров'я годуючих жінок, такі лікарські засоби рекомендується вживати, якщо очікуваний результат від застосування даного лікарського препарату переважає над всілякими ризиками. Щоб уникнути несприятливих наслідків, будь-який медикаментозний препарат слід вживати після консультації з провідним фахівцем. -

 Значення "З обережністю" вказує на те, що вибраний препарат може чинити підвищений негативний вплив на здоров'я алергіків, такі лікарські засоби рекомендується вживати, якщо очікуваний результат від застосування цього лікарського препарату переважає над всілякими ризиками. Щоб уникнути несприятливих наслідків, будь-який медикаментозний препарат слід вживати після консультації з провідним фахівцем.
Значення "З обережністю" вказує на те, що вибраний препарат може чинити підвищений негативний вплив на здоров'я алергіків, такі лікарські засоби рекомендується вживати, якщо очікуваний результат від застосування цього лікарського препарату переважає над всілякими ризиками. Щоб уникнути несприятливих наслідків, будь-який медикаментозний препарат слід вживати після консультації з провідним фахівцем. -

 Значення "Можна" вказує на те, що вибраний препарат має мінімальний ризик для здоров'я діабетиків і результат, очікуваний від вживання лікарського засобу, переважає над можливими ризиками. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем.
Значення "Можна" вказує на те, що вибраний препарат має мінімальний ризик для здоров'я діабетиків і результат, очікуваний від вживання лікарського засобу, переважає над можливими ризиками. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем.
Залишилися питання?
Ми раді допомогти
Характеристики товара
| Виробник | Servier (Франція) |
|---|---|
| Дозування | 25 мг |
| Головний медикамент | Агомелатин |
| Форма товару | Таблетки |
| Спосіб застосування | Оральний |
| Країна виробництва | Франція |
| Взаємодія з алкоголем | Критична |
| Ознака | Імпортний |
| Штрих-код | 5391189190022 |
| Взаємодія з їжею | Не має значення |
| Бренд | Мелітор |
| Умови відпуску | суворо за рецептом |
| Призначення | Для поліпшення роботи нервової системи, мозку |
| Температура зберiгання | не вище 25°C |
Інструкція

Оновлено: 29.03.2026
Перевірено
Інструкція
Мелітор (Melitor) інструкція по застосуванню
Склад
діюча речовина: agomelatine;
1 таблетка містить:
- 25 мг агомелатину;
допомiжнi речовини: лактоза, моногідрат; крохмаль кукурудзяний; повідон; натрію крохмальгліколят (тип А); кислота стеаринова; магнію стеарат; кремнію діоксид колоїдний безводний; гіпромелоза; заліза оксид жовтий (E 172); гліцерин; макрогол 6000; титану діоксид (E 171).
Лікарська форма
Таблетки, вкриті плівковою оболонкою.
Основні фізико-хімічні властивості: оранжево-жовтого кольору, довгастої формитаблетки, вкриті плівковою оболонкою, з голубим тисненням з одного боку.
Фармакотерапевтична група
Психоаналептики. Інші антидепресанти. Код ATX N06A X22.
Фармакологiчнi властивості
Фармакодинаміка.
Механізм дії
Агомелатин – мелатонінергічний агоніст MT1- та MT2-рецепторів та антагоніст 5-HT2c-рецепторів. Дослідження, в рамках яких вивчали зв’язування агомелатину з рецепторами, продемонстрували, що агомелатин не впливає на захоплення моноамінів і не має спорідненості з α- та β-адренергічними, гістамінергічними, холінергічними, допамінергічними та бензодіазепіновими рецепторами.
В експериментальних дослідженнях на тваринах із розладами циркадних ритмів було продемонстровано, що агомелатин ресинхронізує циркадні ритми.
Агомелатин збільшує вивільнення допаміну та норадреналіну, особливо у фронтальних відділах кори головного мозку, та не впливає на екстрацелюлярний рівень серотоніну.
Фармакодинамічні ефекти
В експериментальних дослідженнях на тваринах агомелатин продемонстрував антидепресивний ефект на валідованих моделях депресії (тест безвихідності, відчаю, хронічного легкого стресу), а також на моделях із десинхронізацією циркадних ритмів і моделях, пов’язаних зі стресом і тривожністю.
При застосуванні в людини агомелатин ресинхронізує циркадні ритми; він відновлює фазність сну, спричиняє зниження температури тіла та сприяє секреції мелатоніну.
Клінічна ефективність та безпека
Ефективність і безпека агомелатину при лікуванні великих депресивних епізодів досліджувались у клінічній програмі з участю 7900 пацієнтів.
У шести короткострокових подвійно сліпих плацебо-контрольованих дослідженнях з оцінки ефективності агомелатину при лікуванні великих депресивних епізодів у дорослих пацієнтів агомелатин у дозах 25-50 мг наприкінці терапії (протягом 6-8 тижнів) продемонстрував статистично достовірну ефективність порівняно з плацебо. За результатами оцінювання за шкалою HAMD‑17 відзначалися зміни значення показника первинної кінцевої точки порівняно з початковим рівнем.
Ефективність препарату Мелітор було також продемонстровано в пацієнтів з більш тяжкою депресією (початковий загальний бал за шкалою HAM‑D ≥ 25) за результатами всіх позитивних плацебо-контрольованих досліджень.
Показники відповіді на лікування при застосуванні агомелатину були статистично достовірно вищими порівняно з плацебо.
У шести із семи досліджень із вивчення ефективності Мелітору у гетерогенних популяціях дорослих пацієнтів із депресією було продемонстровано більш високу (2 дослідження) або не нижчу (4 дослідження) ефективність агомелатину порівняно з терапією селективними інгібіторами зворотного захоплення серотоніну/інгібіторами зворотного захоплення серотоніну-норепінефріну (СІЗЗС/ІЗЗСН) (сертралін, есциталопрам, флуоксетин, венлафаксин або дулоксетин). Антидепресивний ефект оцінювали за шкалою HAMD-17 або у якості первинної, або вторинної кінцевої точок.
Довготривалу антидепресивну ефективність агомелатину було продемонстровано в дослідженні з вивчення запобігання виникнення релапсів. За результатами впливу на первинну кінцеву точку – запобігання виникнення релапсів депресії, що вимірювалась часом до виникнення релапсу, агомелатин у дозі 25-50 мг на добу показав статистично достовірну перевагу порівняно з плацебо (р=0,0001). Частота виникнення релапсів протягом 6 місяців подвійно сліпого спостереження становила 22 % та 47 % для агомелатину та плацебо відповідно.
Препарат не впливає на денну пильність та пам’ять здорових добровольців. У пацієнтів із депресією лікування агомелатином у дозі 25 мг подовжувало фазу повільнохвильового сну без впливу на фазу або латентний період швидкого сну. Агомелатин, 25 мг, також скорочує проміжок часу до початку сну (полегшує засинання) та досягнення стану з мінімальною частотою серцевих скорочень. За оцінкою пацієнтів із першого тижня лікування значно покращилися засинання та якість сну без порушення денної активності.
Об’єднаний аналіз досліджень за оціночною шкалою ASEX (Arizona Sexual Experience Scale) продемонстрував, що застосування агомелатину не асоціювалось із сексуальною дисфункцією. У здорових добровольців агомелатин зберігав статеву функцію порівняно з пароксетином.
У клінічних дослідженнях агомелатин не впливав на частоту серцевих скорочень та артеріальний тиск.
У дослідженні з оцінки симптомів відміни за допомогою анкети DESS (Discontinuation Emergent Signs and Symptoms) у пацієнтів із депресією у стадії ремісії агомелатин не спричиняв синдрому відміни після раптового припинення терапії.
Агомелатин не спричиняє залежність, що було визначено в дослідженнях з участю здорових добровольців за результатами тестів із використанням спеціальної візуально-аналогової шкали або анкети ARCI (Addiction Research Center Inventory) із 49 питань.
Плацебо-контрольоване дослідження агомелатину в дозі 25-50 мг на добу тривалістю 8 тижнів з участю пацієнтів літнього віку з депресією (≥ 65 років, N=222, 151 з яких застосовували агомелатин) продемонструвало статистично достовірну різницю у 2,67 бала за загальною шкалою HAM-D (первинна кінцева точка). Рівень показника «відповідь на лікування» був позитивним для агомелатину. У групі пацієнтів віком ≥ 75 років (N=69, 48 з яких застосовували агомелатин) не було отримано достовірних результатів щодо покращення стану. Переносимість агомелатину в пацієнтів літнього віку та в дорослих пацієнтів, молодших за віком, була подібною.
Було проведено спеціальне контрольоване дослідження тривалістю 3 тижні з участю пацієнтів із великими депресивними розладами, які не досягли значного покращення при застосуванні пароксетину (СІЗЗС) або венлафаксину (ІЗЗСН). При переведенні цих пацієнтів на лікування агомелатином, незалежно від того, припинення попередньої терапії відбувалося різко чи поступово, виникали симптоми відміни. Ці симптоми помилково можуть бути розцінені як недостатність раннього ефекту агомелатину.
Відсоток пацієнтів із наявністю хоча б одного симптому відміни протягом 1 тижня після припинення застосування антидепресантів групи СІЗЗС/ІЗЗСН був меншим у групі пацієнтів довготривалого зниження дози (поступове припинення попереднього прийому антидепресантів упродовж 2 тижнів), ніж у групі пацієнтів короткотривалого зменшення дози (поступове припинення попереднього прийому антидепресантів упродовж 1 тижня) та групі пацієнтів різкої зміни лікування (різке припинення прийому): 56,1 %, 62,6 % та 79,8 %, відповідно.
Фармакокінетика.
Всмоктування та біодоступність
Агомелатин швидко і добре (≥ 80 %) всмоктується після перорального застосування. Абсолютна біодоступність є низькою (< 5 % при пероральному застосуванні в терапевтичній дозі); індивідуальна варіабельність є значною. Біодоступність у жінок вища порівняно з чоловіками. Біодоступність підвищується при застосуванні пероральних контрацептивів і зменшується в курців. Максимальна концентрація у плазмі крові досягається протягом 1‒2 годин.
При застосуванні у терапевтичних дозах концентрація агомелатину збільшується пропорційно зі збільшенням дози. При застосуванні у більш високих дозах виникає ефект насичення першою дозою.
Прийом їжі (звичайної або із високим вмістом жирів) не впливає на біодоступність або на рівень всмоктування.
Варіабельність збільшується при прийомі їжі з високим вмістом жирів.
Розподіл у тканинах
Об’єм розподілу в рівноважному стані становить близько 35 л; зв’язування з білками плазми крові становить 95 % незалежно від концентрації та не змінюється з віком і в пацієнтів із порушенням функції нирок, але концентрація вільної фракції збільшується вдвічі у пацієнтів із порушенням функції печінки.
Біотрансформація
Після застосування агомелатин швидко метаболізується, переважно печінковими ферментами CYP1A2; ізоферменти CYP2C9 та CYP2C19 теж беруть участь у метаболізмі, але їх вклад незначний. Основні метаболіти, гідроксильований і диметильований агомелатин, є неактивними та швидко кон’югуються і виводяться із сечею.
Виведення
Виведення з організму є швидким, період напіввиведення із плазми крові становить у середньому 1-2 години. Кліренс високий (приблизно 1,1 мл/хв) і переважно метаболічний. Виводиться переважно із сечею (80 %) у вигляді метаболітів, у той час як кількість виведеної із сечею діючої речовини у незміненому вигляді є незначною. Фармакокінетика не змінюється після багатократного застосування.
Пацієнти з порушенням функції нирок
У пацієнтів із тяжким порушенням функції нирок релевантних змін фармакокінетичних параметрів агомелатину не спостерігалось (n = 8, одноразова доза 25 мг), але пацієнтам із порушенням функції нирок тяжкого або помірного ступеня Мелітор слід призначати з обережністю через обмежену кількість клінічних даних щодо застосування препарату в цій групі пацієнтів (див. розділ «Спосіб застосування та дози»).
Пацієнти з порушенням функції печінки
Спеціальне дослідження з участю пацієнтів із цирозом печінки, хронічним порушенням функції печінки легкого або помірного ступеня (типу А та B за класифікацією Чайлда-П’ю) продемонструвало збільшення (у 70 та 140 разів відповідно) концентрації агомелатину, який застосовували в дозі 25 мг, порівняно з такою у добровольців відповідного віку, маси тіла та звичкою палити без порушення функції печінки (див. розділи «Спосіб застосування та дози», «Протипоказання» та «Особливості застосування»).
Пацієнти літнього віку
Фармакокінетичне дослідження з участю пацієнтів літнього віку (≥ 65 років) показало, що при застосуванні препарату в дозі 25 мг середнє значення показника AUC та Сmax були приблизно в 4 та 13 разів вищі у пацієнтів віком ≥ 75 років порівняно з такими у пацієнтів віком < 75 років. Оцінити фармакокінетику агомелатину при застосуванні в дозі 50 мг у даній популяції неможливо через недостатню кількість даних. Пацієнти літнього віку не потребують корекції дози.
Етнічні групи
Дані щодо особливостей фармакокінетики агомелатину залежно від расової належності відсутні.
Клінічні характеристики.
Показання
Лікування великих депресивних епізодів у дорослих.
Протипоказання Мелітору
- Гіперчутливість до діючої речовини або будь-якої допоміжної речовини препарату.
- Порушення функції печінки (цироз печінки або активна фаза захворювання печінки) або підвищення рівня трансаміназ більше ніж у 3 рази від верхньої межі показників норми (див. розділи «Спосіб застосування та дози» та «Особливості застосування»).
- Застосування у комбінації з сильнодіючими інгібіторами CYP1A2 (флувоксамін, ципрофлоксацин) (див. розділ «Взаємодія з іншими лікарськими засобами та інші види взаємодій»).
Взаємодія з іншими лікарськими засобами та інші види взаємодій
Можливі види взаємодії агомелатину
Агомелатин метаболізується переважно цитохромами P450 1A2 (CYP1A2) (90 %) та CYP2C9/19 (10 %). Лікарські засоби, які взаємодіють із цими ізоферментами, можуть знижувати або підвищувати біодоступність агомелатину.
Флувоксамін, сильнодіючий інгібітор CYP1A2 та помірний інгібітор CYP2C9, значно інгібує метаболізм агомелатину, що призводить до 60-кратного (у діапазоні 12-412) збільшення концентрації агомелатину. Таким чином, одночасне застосування Мелітору із сильнодіючими інгібіторами CYP1A2 (флувоксамін, ципрофлоксацин) протипоказане.
Комбінація агомелатину з естрогенами (помірні інгібітори CYP1A2) призводить до підвищення концентрації агомелатину в декілька разів. Незважаючи на те, що при одночасному застосуванні агомелатину з естрогенами у 800 пацієнтів не було виявлено будь-якого особливого сигналу з безпеки, призначати агомелатин з іншими помірними інгібіторами CYP1A2 (пропранолол, еноксацин) слід з обережністю до одержання більшого досвіду застосування вищезазначеної комбінації (див. розділ «Особливості застосування»).
Рифампіцин, індуктор усіх трьох цитохромів, що беруть участь у метаболізмі агомелатину, може зменшувати біодоступність агомелатину.
Паління стимулює індукцію CYP1A2 та зменшує біодоступність агомелатину, особливо у затятих курців (≥ 15 сигарет/добу) (див. розділ «Фармакокінетика»).
Здатність агомелатину впливати на інші лікарські засоби
In vivoагомелатин не активує ізоферменти системи CYP450. Агомелатин не інгібує ані CYP1A2 in vivo, ані інші ферменти CYP450 in vitro. Як наслідок, він не впливає на концентрацію лікарських засобів, які метаболізуються за допомогою CYP450.
Інші лікарські засоби
У клінічних дослідженнях І фази в цільовій групі пацієнтів не було одержано даних щодо фармакокінетичної та фармакодинамічної взаємодій із лікарськими засобами, які можна одночасно призначати з Мелітором®: бензодіазепіни, літій, пароксетин, флуконазол і теофілін.
Алкоголь
Не рекомендується вживати алкоголь під час лікування агомелатином.
Електрошокова терапія (ЕШТ)
Досвід застосування агомелатину одночасно з ЕШТ відсутній. Дослідження на тваринах не виявили властивостей агомелатину підвищувати судомну готовність. Таким чином, малоймовірно, що одночасне проведення ЕШТ та лікування агомелатином може призвести до будь-якого клінічно значущого ускладнення.
Особливості застосування препарату
Моніторинг функції печінки
При застосуванні агомелатину у післяреєстраційному періоді повідомлялося про виникнення у пацієнтів випадків порушення функції печінки, включаючи печінкову недостатність (повідомлялося про поодинокі випадки з летальними наслідками або трансплантацією печінки у пацієнтів із факторами ризику порушення функції печінки), підвищення рівня печінкових ферментів більше ніж у 10 разів порівняно з верхньою межею норми, гепатит і жовтяницю (див. розділ «Побічні реакції»). Більшість із них виникла протягом перших місяців лікування. Ураження печінки має переважно гепатоцелюлярний характер з підвищенням рівня сироваткових трансаміназ, який зазвичай повертається до норми при припиненні застосування агомелатину.
Мелітор слід призначати з обережністю та ретельно наглядати за всіма пацієнтами протягом періоду лікування, особливо при наявності факторів ризику порушення функції печінки або в разі одночасного застосування лікарських засобів, що можуть зумовити виникнення порушень функції печінки.
До початку лікування
Пацієнтам із такими факторами ризику порушення функції печінки як ожиріння/надлишкова маса тіла/неалкогольний жировий гепатоз печінки, цукровий діабет, порушення, пов’язані з вживанням алкоголю, та/або зловживання алкоголем або пацієнтам, які застосовують супутні лікарські засоби, що можуть зумовити виникнення порушень функції печінки, лікування Мелітором призначати тільки після ретельної оцінки користі та ризику від застосування.
До початку лікування всім пацієнтам необхідно проводити печінкові проби та терапію не слід розпочинати для пацієнтів із початковим рівнем аланінамінотрансферази (АЛТ) та/або аспартатамінотрансферази (АСТ), що перевищує верхню межу норми в 3 рази (див. розділ «Протипоказання»). Пацієнтам із підвищеним рівнем трансаміназ до початку лікування (за умови підвищення рівня трансаміназ не більше, ніж у 3 рази від верхньої межі норми) Мелітор® слід застосовувати з обережністю.
Частота проведення печінкових проб:
- до початку лікування;
- та потім:
- приблизно через 3 тижні;
- приблизно через 6 тижнів (наприкінці гострої фази);
- приблизно через 12 тижнів та 24 тижні (наприкінці фази підтримувальної терапії);
і надалі у разі наявності клінічних показань.
- при збільшенні дози слід знову провести печінкові тести з тією ж частотою, що й на початку лікування.
Будь-який пацієнт, у якого розвинулося та було виявлено підвищення рівня трансаміназ у плазмі крові, має пройти повторний тест на визначення функції печінки впродовж 48 годин.
Протягом періоду лікування
Застосування препарату Мелітор слід негайно припинити, якщо:
- у пацієнта розвинулися симптоми потенційного порушення функції печінки (такі як темна сеча, випорожнення світлого кольору, пожовтіння шкіри/очей, біль у верхній правій частині живота, нові випадки виникнення тривалої втоми нез’ясованої етіології);
- рівень сироваткових трансаміназ перевищує верхню межу норми у 3 рази.
Після припинення прийому Мелітору необхідно повторити проведення печінкових тестів, доки показники сироваткових трансаміназ не нормалізуються.
Люди віком від 75 років
Ефекту від застосування агомелатину у пацієнтів віком ≥ 75 років доведено не було, тому пацієнтам цієї вікової групи не слід застосовувати агомелатин (див. розділи «Спосіб застосування та дози» та «Фармакодинаміка»).
Пацієнти літнього віку з деменцією
Мелітор не слід застосовувати для лікування великих депресивних епізодів у пацієнтів літнього віку з деменцією, оскільки безпеку та ефективність Мелітору у цій групі пацієнтів встановлено не було.
Біполярний розлад/манія/гіпоманія
Мелітор слід застосовувати з обережністю для лікування пацієнтів із наявністю в анамнезі біполярного розладу, манії або гіпоманії, та його необхідно відмінити в разі виникнення в пацієнта маніакальних симптомів (див. розділ «Побічні реакції»).
Суїцид/суїцидальні думки
Депресія супроводжується підвищенням ризику виникнення суїцидальних думок, заподіянням собі шкоди та суїциду (суїцидальні прояви). Цей ризик зберігається до досягнення клінічно значущої ремісії. Оскільки стан пацієнта може не покращитись у перші декілька або більше тижнів лікування, необхідно здійснювати ретельне спостереження за пацієнтом до покращення стану. Загальний клінічний досвід свідчить про те, що ризик суїциду може підвищуватися на ранніх стадіях покращення стану.
Пацієнти із наявністю в анамнезі суїцидальних проявів, а також пацієнти, у яких відзначається високий рівень суїцидального мислення перед початком лікування, є групою підвищеного ризику суїцидальних думок або суїцидальних спроб і їм слід перебувати під ретельним наглядом під час лікування. Мета-аналіз плацебо-контрольованих клінічних досліджень антидепресантів з участю дорослих пацієнтів із психічними розладами показав підвищення ризику суїцидальної поведінки при застосуванні антидепресантів порівняно з плацебо у групі пацієнтів віком до 25 років.
Під час лікування, особливо на ранніх етапах та після зміни дозування, необхідно здійснювати ретельний нагляд за пацієнтами, зокрема тими, які відносяться до групи високого ризику. Пацієнтів (та осіб, які піклуються про них) слід попередити про необхідність відстеження будь-яких ознак клінічного погіршення, виникнення суїцидальної поведінки або думок і незвичних змін у поведінці, а також негайного звернення до лікаря при наявності цих симптомів.
Застосування в комбінації з інгібіторами CYP1А2 (див. розділи «Протипоказання» та «Взаємодiя з iншими лiкарськими засобами та інші види взаємодій»)
Мелітор слід з обережністю призначати в комбінації з помірними інгібіторами CYP1А2 (пропранолол, еноксацин), що може призвести до підвищення концентрації агомелатину.
Непереносимість лактози
До складу Мелітору входить лактоза. Пацієнтам із рідкісною спадковою непереносимістю галактози, загальним дефіцитом лактази або мальабсорбцією глюкози-галактози не слід приймати цей препарат.
Рівень натрію
Мелітормістить менше 1 ммоль натрію (23 мг) на таблетку, тобто майже вільний від натрію.
Застосування у період вагітності або годування груддю
Вагітність
З метою попередження будь-яких ризиків бажано уникати застосування Мелітору у період вагітності. Дані щодо застосування агомелатину вагітним жінкам відсутні або обмежені (менше 300 випадків). Дослідження на тваринах не виявили прямих або непрямих шкідливих ефектів агомелатину на перебіг вагітності, розвиток ембріона/плода, пологи або постнатальний розвиток.
Годування груддю
Невідомо, чи проникає агомелатин/метаболіти у грудне молоко. Наявні фармакодинамічні/токсикологічні дані, одержані при проведенні досліджень на тваринах, продемонстрували, що агомелатин/метаболіти проникають у грудне молоко. Ризик для новонароджених/немовлят виключати не можна. Рішення щодо припинення годування груддю або припинення/утримання від терапії Мелітором® слід приймати, враховуючи користь від годування груддю для дитини та користь від лікування для матері.
Фертильність
Дослідження з репродуктивності на тваринах показали відсутність впливу агомелатину на фертильність.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами
Агомелатин має незначний вплив на здатність керувати автомобілем або працювати з механізмами. З огляду на те, що запаморочення та сонливість є частими побічними реакціями на препарат, пацієнтам слід бути обережними при керуванні автотранспортом або роботі з механізмами.
Спосіб застосування та дози Мелітор
- Спосіб застосування
Для перорального застосування.
Мелітор, таблетки, вкриті плівковою оболонкою, можна застосовувати незалежно від прийому їжі.
- Дозування
Рекомендована доза становить 25 мг 1 раз на добу, перед сном.
Якщо через 2 тижні після початку терапії покращання клінічного стану є недостатнім, дозу можна підвищити до 50 мг 1 раз на добу, тобто 2 таблетки по 25 мг, які необхідно приймати одночасно перед сном.
При прийнятті рішення щодо збільшення дози слід ураховувати зростання ризику підвищення рівня трансаміназ. Збільшення дози до 50 мг необхідно проводити на індивідуальній основі для кожного пацієнта після оцінки показника «користь/ризик» із обов’язковим проведенням печінкових проб.
Усім пацієнтам необхідно проводити печінкові проби до початку лікування. Лікування не слід розпочинати, якщо рівень трансаміназ перевищує верхню межу норми у 3 рази (див. розділи «Протипоказання» та «Особливості застосування»).
Під час лікування необхідно періодично контролювати рівень трансаміназ: приблизно через 3 тижні, 6 тижнів (завершення гострої фази), через 12 тижнів та 24 тижні (завершення фази підтримувальної терапії) і надалі у разі наявності клінічних показань (див. розділ «Особливості застосування»). Лікування слід припинити, якщо рівень трансаміназ втричі перевищить верхню межу норми (див. розділи «Протипоказання» та «Особливості застосування»).
При збільшенні дози слід знову провести печінкові тести з тією ж частотою, що і на початку лікування.
- Тривалість лікування
Пацієнтам із депресією слід проходити лікування впродовж щонайменше 6 місяців для забезпечення зникнення у них симптомів.
Перехід від терапії антидепресантами групи селективних інгібіторів зворотного захоплення серотоніну/інгібіторів зворотного захоплення серотоніну і норепінефрину (СІЗЗС/ІЗЗСН) до агомелатину
У пацієнтів можуть спостерігатися симптоми відміни після припинення прийому антидепресантів групи СІЗЗС/ІЗЗСН. З метою уникнення цих симптомів необхідно враховувати рекомендації щодо припинення лікування, що містяться в інструкції для медичного застосування лікарського засобу, який застосовує пацієнт. Терапію агомелатином можна розпочати одразу паралельно зі зниженням дози антидепресанта (див. розділ «Фармакодинаміка»).
- Припинення лікування
У разі прийняття рішення щодо припинення лікування потреби у поступовому зниженні дози немає.
Особливі групи пацієнтів
- Пацієнти літнього віку
Безпека та ефективність агомелатину (25-50 мг/добу) були доведені для пацієнтів літнього віку з депресією (< 75 років). У групі пацієнтів віком ≥ 75 років не було отримано достовірних результатів. Тому пацієнтам цієї вікової групи не слід застосовувати агомелатин (див. розділи «Особливості застосування» та «Фармакодинаміка»). Потреби в корекції дози залежно від віку немає (див. розділ «Фармакокінетика»).
- Пацієнти з порушенням функції нирок
У пацієнтів із тяжким порушенням функції нирок релевантних змін фармакокінетичних параметрів агомелатину не спостерігалось. Однак кількість клінічних даних щодо застосування агомелатину у пацієнтів із депресією та порушенням функції нирок тяжкого або помірного ступеня є обмеженою. Отже, таким пацієнтам агомелатин слід призначати з обережністю.
- Пацієнти з порушенням функції печінки
Застосування агомелатину протипоказано пацієнтам із порушенням функції печінки (див. розділи «Протипоказання», «Особливості застосування» та «Фармакокінетика»).
Діти
Не рекомендується призначати Мелітор для лікування депресії в дітей, оскільки безпека та ефективність даного препарату не були встановлені в цій групі пацієнтів. Дані відсутні. У клінічних дослідженнях з участю дітей і підлітків при застосуванні інших антидепресантів виникнення суїцидальної поведінки (суїцидальні спроби та суїцидальні думки) і ворожого ставлення (переважно агресія, опозиційна поведінка та гнів) спостерігалось частіше порівняно з пацієнтами, які приймали плацебо.
Передозування
Симптоми
Існує обмежена кількість даних щодо випадків передозування агомелатином. При передозуванні агомелатином повідомлялося про виникнення болю в епігастральній ділянці, сонливості, втоми, ажитації, тривожного стану, напруженості, запаморочення, ціанозу або нездужання. Було зафіксовано 1 випадок прийому 2450 мг агомелатину − одужання настало спонтанно без кардіоваскулярних та біологічних відхилень.
Лікування
Будь-які специфічні антидоти агомелатину невідомі. Лікування при передозуванні має складатись із симптоматичної терапії та звичайного нагляду за станом пацієнта. Медичне спостереження рекомендується проводити у спеціалізованому закладі.
Побічні реакції Мелітору
Резюме профілю безпеки
Побічні реакції зазвичай виникали під час перших 2 тижнів лікування та були слабко або помірно виражені. Найчастішими побічними реакціями були головний біль, нудота та запаморочення. Ці побічні реакції зазвичай мали тимчасовий характер і, як правило, не призводили до припинення терапії.
Перелік побічних реакцій
Нижченаведена таблиця містить побічні реакції, виявлені під час плацебо-контрольованих клінічних досліджень та випробувань з використанням активного контролю.
Побічні реакції зазначені нижче з такою частотою виникнення: дуже часто (≥ 1/10); часто (від ≥ 1/100 до < 1/10); нечасто (від ≥ 1/1000 до < 1/100); рідко (від ≥ 1/10000 до < 1/1000); дуже рідко (< 1/10000); частота невідома (не може бути визначена за наявними даними). Частота не була скоригована для групи плацебо.
|
Класифікація за системами органів |
Частота |
Побічна реакція |
|
З боку психіки |
Часто |
Тривожність |
|
Незвичні сновидіння* |
||
|
Нечасто |
Суїцидальні думки чи поведінка (див. розділ «Особливості застосування») |
|
|
Ажитація та пов’язані з нею симптоми* (такі як дратівливість і неспокій) |
||
|
Агресивність* |
||
|
Жахливі сновидіння* |
||
|
Манія/гіпоманія* Ці симптоми можуть бути зумовлені відповідним захворюванням (див. розділ «Особливості застосування») |
||
|
Сплутаність свідомості* |
||
|
Рідко |
Галюцинації* |
|
|
З боку нервової системи |
Дуже часто |
Головний біль |
|
Часто |
Запаморочення |
|
|
Сонливість |
||
|
Безсоння |
||
|
Нечасто |
Мігрень |
|
|
Парестезія |
||
|
Синдром неспокійних ніг* |
||
|
Рідко |
Акатизія* |
|
|
З боку органів зору |
Нечасто |
Нечіткість зору |
|
З боку органів слуху та лабіринту |
Нечасто |
Дзвін у вухах* |
|
З боку шлунково-кишкового тракту |
Часто |
Нудота |
|
Діарея |
||
|
Запор |
||
|
Біль в абдомінальній ділянці живота |
||
|
Блювання* |
||
|
З боку гепатобіліарної системи |
Часто |
Підвищення рівня аланінамінотрансферази (АЛТ) та/або аспартатамінотрансферази (АСТ) (у клінічних дослідженнях підвищення рівня АЛТ та/або АСТ більше ніж у 3 рази від верхньої межі норми спостерігалось у 1,2 % пацієнтів, які отримували агомелатин у дозі 25 мг/добу, та у 2,6 % пацієнтів, які отримували агомелатин у дозі 50 мг/добу, порівняно з 0,5 % пацієнтів, що отримували плацебо) |
|
Нечасто |
Підвищення рівня гамма-глутамілтрансферази* (ГГТ) (більш ніж у 3 рази від верхньої межі норми) |
|
|
Рідко |
Гепатит |
|
|
Підвищення рівня лужної фосфатази* (більш ніж у 3 рази від верхньої межі норми) |
||
|
Печінкова недостатність* (1) |
||
|
Жовтяниця* |
||
|
З боку шкіри і підшкірної клітковини |
Нечасто |
Гіпергідроз |
|
Екзема |
||
|
Свербіж* |
||
|
Кропив’янка* |
||
|
Рідко |
Еритематозні висипання |
|
|
Набряк обличчя та ангіоневротичний набряк* |
||
|
З боку опорно-рухової системи та сполучної тканини |
Часто |
Біль у спині |
|
Нечасто |
Міалгія* |
|
|
З боку сечовидільної системи |
Рідко |
Затримка сечовипускання* |
|
Загальні розлади та реакції у місці введення |
Часто |
Втома |
|
Результати лабораторних досліджень |
Часто |
Збільшення маси тіла* |
|
Нечасто |
Зменшення маси тіла* |
* Частота проявів побічних реакцій, виявлених за допомогою спонтанних повідомлень, розрахована за даними клінічних досліджень.
(1) Повідомлялося про поодинокі летальні випадки або випадки трансплантації печінки у пацієнтів із факторами ризику порушення функції печінки.
Звіт про підозрювані побічні реакції
Звітування про підозрювані побічні реакції у післяреєстраційному періоді лікарського засобу є важливим. Це дозволяє вести безперервний моніторинг співвідношення користі/ризику застосування препарату. Спеціалісти в галузі охорони здоров’я зобов’язані повідомляти через національну систему звітності про будь-які випадки підозрюваних побічних реакцій.
Термін придатності
3 роки.
Умови зберігання
Не потребує особливих умов зберігання. Зберігати у недоступному для дітей місці.
Упаковка
По 14 таблеток, вкритих плівковою оболонкою, у блістері з алюмінієвої фольги та ПВХ‑плівки.
По 1 або 2, або 4 блістери в коробці з картону пакувального.
Категорія відпуску з аптеки
За рецептом.
Відгуки користувачів
5.0 1 відгук
5 зірок 100% (1)
4 зірки 0% (0)
3 зірки 0% (0)
2 зірки 0% (0)
1 зірка 0% (0)
- ИннессаМелитор хорошо помогает при депрессии, нужно пропить курсом, правда негативно влияет на печень, параллельно пропиваю лекарство для поддержания печени.
Залишити відгук
Дивіться інші товари у категорії:
Зверніть увагу
Інформація/інструкція до препарату носить ознайомчий характер і призначена виключно для інформаційних цілей.