Для поліпшення роботи сайту ми використовуємо файли cookie. Продовжуючи переглядати сайт, ви погоджуєтеся з цим.
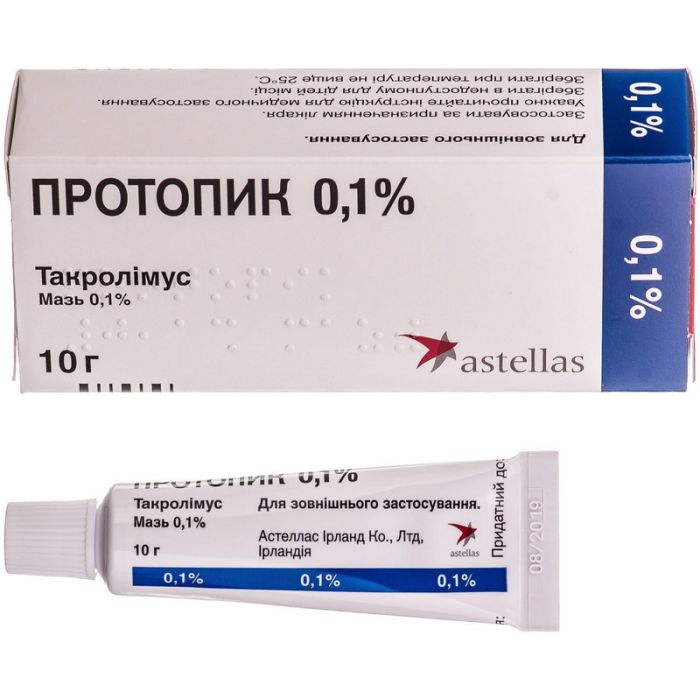
Протопик 0,1% мазь 10 г
687,20 ₴
Ansell Lanka (Шри-Ланка)
Арт.
27911

У список
Протопик 0,1% мазь 10 г
Ansell Lanka (Шри-Ланка)
Увага! Ціни дійсні тільки при покупці онлайн
Ваше місто - Київ?
Ваше місто
Ізмаїл
Товар відсутній в аптеках обраного міста

Самовивіз
Безкоштовно

Кур'єром
Доставка до 48 годин
Безкоштовно від 2000 грн
Рецептурний препарат. Можливий тільки самовивіз з аптеки

Нова Пошта відділення
Доставка від 1 дня
Від 80 грн

Нова Пошта поштомат
Доставка від 1 дня
Від 80 грн

Нова Пошта курʼєр
Доставка від 1 дня
Від 150 грн

Укрпошта відділення
Доставка від 2 днів
Від 52 грн
На сайті
При отриманні
-

 Значення "Можна" вказує на те, що вибраний препарат має мінімальний ризик для здоров'я дорослого населення і результат, очікуваний від вживання лікарського засобу, переважає над можливими ризиками. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем.
Значення "Можна" вказує на те, що вибраний препарат має мінімальний ризик для здоров'я дорослого населення і результат, очікуваний від вживання лікарського засобу, переважає над можливими ризиками. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем. -


-
 Значення "Не можна" вказує на те, що вибраний препарат має максимальний ризик для здоров'я вагітних жінок і, відповідно, ризики від вживання даного лікарського препарату переважають над очікуваним результатом. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем.
Значення "Не можна" вказує на те, що вибраний препарат має максимальний ризик для здоров'я вагітних жінок і, відповідно, ризики від вживання даного лікарського препарату переважають над очікуваним результатом. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем. -
 Значення "Не можна" вказує на те, що вибраний препарат має максимальний ризик для здоров'я годуючих жінок, і відповідно, ризики від вживання даного лікарського препарату переважають над очікуваним результатом. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем.
Значення "Не можна" вказує на те, що вибраний препарат має максимальний ризик для здоров'я годуючих жінок, і відповідно, ризики від вживання даного лікарського препарату переважають над очікуваним результатом. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем. -

 Значення "Можна" вказує на те, що вибраний препарат має мінімальний ризик для здоров'я алергіків і результат, очікуваний від вживання лікарського засобу, переважає над можливими ризиками. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем.
Значення "Можна" вказує на те, що вибраний препарат має мінімальний ризик для здоров'я алергіків і результат, очікуваний від вживання лікарського засобу, переважає над можливими ризиками. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем. -

 Значення "Можна" вказує на те, що вибраний препарат має мінімальний ризик для здоров'я діабетиків і результат, очікуваний від вживання лікарського засобу, переважає над можливими ризиками. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем.
Значення "Можна" вказує на те, що вибраний препарат має мінімальний ризик для здоров'я діабетиків і результат, очікуваний від вживання лікарського засобу, переважає над можливими ризиками. Щоб уникнути негативних наслідків, будь-який медикаментозний препарат слід застосовувати після консультації з лікарем.
Залишилися питання?
Ми раді допомогти
Характеристики товара
| Виробник | Ansell Lanka (Шри-Ланка) |
|---|---|
| Дозування | 1 мг/г |
| Головний медикамент | Такролімус |
| Форма товару | Мазь |
| Маса | 10 г |
| Спосіб застосування | Зовнішній |
| Країна виробництва | Шрі-Ланка |
| Ознака | Імпортний |
| Штрих-код | 4607098450616 |
| Бренд | Протопик |
| Умови відпуску | за рецептом |
| Призначення | При екземі та дерматиті |
| Температура зберiгання | не вище 25°C |
Інструкція

Оновлено: 10.04.2026
Перевірено
Інструкція
Протопик (Protopic) інструкція по застосуванню
Склад
діюча речовина: такролімус;
1 г мазі містить:
- такролімусу (у вигляді моногідрату) 0,3 мг або 1 мг;
допоміжні речовини: парафін білий м’який, олія мінеральна, пропіленкарбонат, віск білий, парафін, бутилгідрокситолуол (E 321), альфа-токоферол.
Лікарська форма
Мазь.
Основні фізико-хімічні властивості:
мазь від білого до злегка жовтуватого кольору.
Фармакотерапевтична група
Дерматологічні засоби. Код АТХ D11A Н01.
Фармакологічні властивості
Фармакодинаміка.
За допомогою зв’язування зі специфічним цитоплазматичним білком імунофіліном (FKBP12) такролімус інгібує кальційзалежну передачу сигналу Т-лімфоцитам, перешкоджаючи їх активації та подальшому синтезу IL-2, IL-3, IL-4, IL-5 та інших цитокінів, таких як GM-CSF, ТNF-α та IFN-γ.
У ході досліджень in vitro у шкірі здорової людини такролімус інгібував опосередковану клітинами Лангерганса стимуляцію Т-лімфоцитів. Було також показано, що такролімус перешкоджає вивільненню медіаторів запалення з опасистих клітин, базофілів та еозинофілів.
У хворих на атопічний дерматит очищення шкіри під час лікування такролімусом у формі мазі супроводжувалось зниженням експресії Fc-рецептора на клітинах Лангерганса та гальмуванням їх стимулюючого впливу на Т-лімфоцити.
Такролімус в лікарській формі мазі не впливає на синтез колагену, таким чином, не спричиняє атрофії шкіри.
Фармакокінетика.
Абсорбція. Дані, отримані від здорових добровольців, показали, що рівень системного впливу такролімусу після разового чи багаторазового місцевого застосування мазі такролімусу відсутній або мінімальний.
У більшості пацієнтів із атопічним дерматитом (дорослих та дітей), які одноразово чи повторно застосовували мазь такролімусу (0,03 – 0,1%), його концентрація у крові < 1 нг/мл. Якщо концентрація у крові перевищувала 1 нг/мл, це явище було тимчасовим. Рівень системного впливу підвищувався зі збільшенням площі уражених ділянок. Однак швидкість та ступінь місцевої абсорбції такролімусу зменшувались із загоєнням шкіри. У дорослих та дітей, в середньому на 50 % площі тіла яких застосовували препарат, рівень системного впливу (тобто AUC) такролімусу був приблизно у 30 разів менший, ніж рівень системного впливу імунодепресантів після їх перорального прийому пацієнтами з трансплантованою ниркою або печінкою. Найнижча концентрація такролімусу у крові, при якій проявляється системна дія, невідома.
Кумуляції препарату при тривалому застосуванні (до 1 року) у дітей та дорослих не відзначалось.
Розподіл в організмі. У зв'язку з тим, що системна абсорбція мазі такролімусу низька, висока здатність зв'язування його з білками плазми (> 98,8 %) розглядається як клінічно не значуща. При застосуванні мазі такролімусу препарат діє місцево та характеризується мінімальною абсорбцією в системний кровотік.
Метаболізм. Такролімус не метаболізується в шкірі. При попаданні в системний кровообіг такролімус значною мірою метаболізується в печінці за допомогою CYP3A4.
Виведення. При внутрішньовенному введенні такролімус показав низький рівень кліренсу. Середній загальний кліренс становить приблизно 2,25 л/год. Печінковий кліренс абсорбованого в системний кровотік препарату може зменшуватись у пацієнтів з тяжкою печінковою недостатністю або при одночасному прийомі інгібіторів CYP3A4.
При багаторазовому місцевому застосуванні мазі такролімусу період напіввиведення становить 75 годин у дорослих та 65 годин у дітей.
Діти.
Фармакокінетичні властивості такролімусу після місцевого застосування подібні до зареєстрованих у дорослих, включаючи мінімальний рівень системного впливу та відсутність кумуляції (див. вище).
Показання
Лікування атопічного дерматиту у дітей віком від 2 років – мазь Протопик 0,03 %, у дорослих та підлітків віком від 16 років – мазь Протопик 0,03 % та 0,1 % .
Лікування загострень
Дорослі та підлітки (віком від 16 років)
Лікування атопічного дерматиту середнього та тяжкого ступеня у дорослих та підлітків (віком від 16 років), які неадекватно реагують або нечутливі до традиційних методів лікування, зокрема до лікування топічними кортикостероїдами.
Діти (віком від 2 до 16 років)
Лікування атопічного дерматиту середнього та тяжкого ступеня у дітей віком від 2 до 16 років, які неадекватно реагують на традиційні методи лікування, зокрема топічними кортикостероїдами.
Профілактика виникнення загострень
Профілактичне лікування атопічного дерматиту середнього та тяжкого ступеня для запобігання раптових загострень хвороби та подовження тривалості періодів без загострень у пацієнтів з високою частотою виникнення рецидивів (4 або більше разів на рік), які мали первинну реакцію на максимум 6-тижневий курс лікування маззю (двічі на день) – повне, майже повне або незначне загоєння уражень.
Протипоказання Протопику
Гіперчутливість до такролімусу, макролідів або допоміжних речовин.
Взаємодія з іншими лікарськими засобами та інші види взаємодій.
Формальні дослідження взаємодій топічного препарату для мазі такролімусу не проводилися.
Такролімус не метаболізується в шкірі людини, що практично виключає можливість взаємодії з іншими препаратами в шкірі, що могло б вплинути на метаболізм такролімусу.
Системно доступний такролімус метаболізується за допомогою печінкового цитохрому P450 3A4 (CYP3A4). Рівень системного впливу у разі місцевого застосування мазі такролімусу низький (< 1 нг/мл) та навряд чи може змінитися внаслідок одночасного прийому відомих інгібіторів CYP3A4. Однак можливість взаємодії виключати не можна, і тому одночасний системний прийом відомих інгібіторів CYP3A4 (таких як еритроміцин, ітраконазол, кетоконазол, дилтіазем) пацієнтами з великими ділянками ураження та/або еритродермією потрібно проводити обережно.
Діти.
Було проведено дослідження лікарської взаємодії з кон’югованою з білком вакциною проти менінгококу серологічної групи С у дітей віком 2 – 11 років. Не спостерігалося жодного впливу на вакцинацію, на утворення імунної пам’яті або гуморальний чи клітинний імунітет.
Особливості застосування препарату
Мазь Протопик не можна застосовувати хворим з уродженим або набутим імунодефіцитом або пацієнтам, які приймають імуносупресивні препарати.
Вплив мазі Протопик на імунну систему дітей віком до 2 років не встановлений (див. розділ «Показання»).
Під час застосування мазі необхідно мінімізувати попадання на шкіру сонячних променів, уникати ультрафіолетового опромінення в солярії, терапії УФ-променями Б та А в комбінації з псораленом (PUVA-терапія). Лікар повинен порадити пацієнтам належний спосіб захисту від сонця, наприклад: мінімізація часу, проведеного на сонці, використання сонцезахисних препаратів та прикриття шкіри належним одягом. Мазь Протопик не слід застосовувати на уражені ділянки, які розглядаються як потенційно злоякісні або передракові.
Протягом 2 годин на ділянки шкіри, куди наносили мазь Протопик, не можна застосовувати пом’якшувальні засоби. Одночасне застосування інших препаратів місцевого застосування, а також системних стероїдів або імунодепресантів не вивчалося.
Ефективність та безпеку застосування мазі Протопик при лікуванні інфікованого атопічного дерматиту не оцінювали. Перед призначенням мазі Протопик необхідно усунути інфекцію на ділянках лікування. Пацієнти з атопічним дерматитом схильні до розвитку поверхневих інфекцій шкіри. Лікування маззю Протопик може бути пов’язане з підвищеним ризиком виникнення фолікуліту та герпетичних вірусних інфекцій (вірус герпесу (герпетична екзема), простий герпес (герпетична пропасниця), варицеліформний пустульоз Капоші) (див. розділ «Побічні реакції»). За наявності цих інфекцій необхідно оцінити співвідношення ризику та користі застосування Протопику. Ймовірність місцевого пригнічення імунітету (що може призвести до інфекцій або шкірних злоякісних новоутворень) у довгостроковій перспективі (більше кількох років) невідома.
Протопик містить діючу речовину такролімус, інгібітор кальциневрину. У пацієнтів після трансплантації тривала системна дія сильних імунодепресантів та системний прийом інгібіторів кальциневрину можуть асоціюватись із підвищеним ризиком розвитку лімфом та злоякісних утворень в шкірі. Є інформація про випадки виникнення злоякісних новоутворень, включаючи нашкірні (зокрема шкірна Т-клітинна лімфома) та інші лімфоми і рак шкіри, у пацієнтів, які застосовували мазь такролімусу (див. розділ «Побічні реакції»). У пацієнтів з атопічним дерматитом, яких лікували Протопиком, не було виявлено значних системних рівнів такролімусу.
Під час клінічних випробувань стало відомо про рідкі випадки лімфаденопатії (0,8 %). Більшість цих випадків була пов’язана з інфекціями (шкіри, дихальних шляхів, зубів), які лікувались відповідними антибіотиками. Пацієнти після трансплантації, які проходять курс прийому імунодепресантів (наприклад системного такролімусу), мають підвищений ризик розвитку лімфоми; тому за пацієнтами, які застосовують Протопик та у яких розвинулась лімфаденопатія, необхідний нагляд, щоб переконатися, що лімфаденопатія зникає. При наявності лімфаденопатії на початку лікування потрібні відповідні лабораторні дослідження та постійний нагляд. У разі стійкої лімфаденопатії необхідно визначити її етіологію. За відсутності чіткої етіології лімфаденопатії або за наявності гострого інфекційного мононуклеозу застосування Протопику необхідно припинити.
Потрібно уникати потрапляння мазі в очі та на слизові оболонки. У разі випадкового потрапляння на ці ділянки мазь необхідно ретельно витерти та/або змити водою.
Використання мазі Протопик під оклюзійними пов’язками не вивчалося і тому не рекомендоване.
Як і при використанні інших препаратів місцевого застосування, пацієнти повинні мити руки після нанесення, якщо лікування шкіри рук не потрібне.
Такролімус значною мірою метаболізується у печінці, і хоча його концентрація в крові при зовнішньому застосуванні дуже низька, хворі з печінковою недостатністю повинні застосовувати мазь із обережністю.
Не рекомендується застосовувати Протопик пацієнтам з дефектами епідермального бар’єра, такими як синдром Нетертона, ламілярний іхтіоз, еритродермія або шкірна реакція ТПХ (трансплантат проти хазяїна). Ці захворювання шкіри можуть спричинити збільшення системної абсорбції такролімусу. Також не рекомендується пероральне застосування такролімусу для лікування цієї патології шкіри. У постмаркетинговий період повідомлялося про випадки підвищеного рівня такролімусу у пацієнтів з цими захворюваннями.
З обережністю слід застосовувати Протопик хворим з обширним ураженням шкіри протягом тривалого періоду, особливо дітям (див. розділ «Спосіб застосування та дози»).
Будь-які нові утворення, окрім власне атопічного дерматиту, на ділянках шкіри, куди наносили мазь, повинен обстежити лікар.
Якщо симптоми атопічного дерматиту не зменшуються, лікування повинно бути переглянуто.
Мазь Протопик містить бутилгідрокситолуол (E 321), що може спричинити місцеві шкірні реакції (наприклад, контактний дерматит) або подразнення очей і слизових оболонок.
Застосування у період вагітності або годування груддю.
Немає даних щодо застосування мазі такролімусу вагітними жінками. Дослідження на тваринах показали, що системне застосування призводить до репродуктивної токсичності. Потенційний ризик для людини невідомий.
Мазь Протопик не слід використовувати у період вагітності, за винятком вкрай невідкладних випадків.
Годування груддю
Клінічні дані доводять, що після системного застосування такролімус проникає в грудне молоко. Хоча клінічні дані показали, що рівень системного впливу від застосування мазі такролімусу низький, годування груддю під час застосування мазі Протопик слід припинити.
Фертильність
Дані щодо фертильності відсутні.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Препарат застосовується місцево та не впливає чи впливає незначно на здатність керувати автомобілем та працювати з іншими механізмами.
Спосіб застосування та дози Протопик
Мазь Протопик необхідно наносити тонким шаром на уражені або ті ділянки шкіри, що найчастіше уражуються. Мазь можна наносити на будь-які частини тіла (обличчя, шию тощо), у тому числі на згинальні поверхні. Необхідно уникати потрапляння мазі на слизові оболонки. Мазь не слід наносити під оклюзійні пов’язки, оскільки такий спосіб застосування не досліджений (див. розділ «Особливості застосування»).
Лікування загострень
Протопик можна застосовувати як короткочасно, так і протягом тривалого періоду, у вигляді повторюваних курсів терапії. Тривале лікування не повинно бути безперервним.
Лікування Протопиком потрібно розпочати при першій появі симптомів і продовжувати до повного, майже повного або значного зникнення уражень на шкірі. Потрібно обробляти маззю кожну пошкоджену ділянку шкіри. Після цього пацієнтів можна переводити на профілактичне лікування (див. далі). При перших ознаках повторного виникнення симптомів хвороби лікування необхідно поновити.
Діти віком від 2 до 16 років
Необхідно застосовувати мазь меншої концентрації (Протопик 0,03%). Курс лікування – двічі на день протягом трьох тижнів. Надалі частоту застосування потрібно зменшити до одного разу на день до повного зникнення уражень на шкірі (див. розділ «Особливості застосування»).
Дорослі та підлітки (віком від 16 років)
Лікування потрібно почати з Протопику 0,1% двічі на день та продовжувати до повного зникнення уражень на шкірі. При повторному виникненні симптомів лікування починають знову. Якщо дозволяє клінічний стан, необхідно спробувати зменшити частоту нанесення препарату або застосовувати мазь меншої концентрації (Протопик 0,03%).
Як правило, покращення можна спостерігати протягом першого тижня лікування. Якщо ознаки поліпшення не спостерігаються протягом двох тижнів застосування мазі, необхідно розглянути інші варіанти подальшого лікування.
Пацієнти літнього віку
Окремі дослідження за участю пацієнтів літнього віку не проводилися. Однак клінічний досвід роботи із пацієнтами цієї вікової групи показує, що корекція режиму дозування не потрібна.
Профілактика виникнення загострень
На профілактичне лікування пацієнтів можна переводити після 6-тижневого курсу лікування маззю із застосуванням препарату двічі на день (до повного, майже повного або значного зникнення уражень на шкірі).
Діти віком від 2 до 16 років
Необхідно застосовувати мазь меншої концентрації (Протопик 0,03%). Мазь потрібно застосовувати один раз на день двічі на тиждень (наприклад у понеділок та четвер) на ділянки шкіри, які найчастіше уражаються атопічним дерматитом, для запобігання виникненню загострень. Між застосуваннями мазі потрібно робити 2 – 3 дні перерви.
Після 12 місяців застосування мазі дитині слід тимчасово призупинити лікування для визначення необхідності продовження курсу профілактичної терапії та для оцінки перебігу хвороби.
Дорослі та підлітки (віком від 16 років)
Необхідно застосовувати мазь Протопик 0,1%. Мазь потрібно наносити один раз на день двічі на тиждень (наприклад у понеділок та четвер) на ділянки шкіри, які найчастіше уражаються атопічним дерматитом, для запобігання виникненню загострень. Між застосуваннями мазі потрібно робити 2 – 3 дні перерви.
Після 12 місяців лікування лікар повинен оцінити стан пацієнта та прийняти рішення щодо подальшого профілактичного лікування, оскільки дані стосовно профілактичного лікування тривалістю понад 12 місяців відсутні.
При виникненні ознак загострення необхідно повернутися до застосування препарату двічі на день.
Пацієнти літнього віку
Окремі дослідження за участю пацієнтів літнього віку не проводилися.
Діти.
Мазь Протопик застосовують дітям віком від 2 років.
Передозування
При місцевому застосуванні передозування малоймовірне.
При попаданні всередину необхідно вжити загальноприйнятих заходів, які включають контроль життєво важливих функцій організму та моніторинг загального стану. Стимулювання блювання або промивання шлунка не рекомендується через особливості допоміжних речовин, що містить мазь.
Побічні реакції Протопику
Під час клінічних досліджень у приблизно 50 % пацієнтів виникла небажана реакція у вигляді подразнення шкіри на місці нанесення мазі. Часто виникали відчуття печіння та свербіж, звичайно слабкі або середньої сили, які в основному зникали після першого тижня лікування. Поширеною небажаною реакцією була еритема. Також часто спостерігалися відчуття теплоти, біль, парестезія та висипання. Часто зустрічалась непереносимість алкоголю (почервоніння обличчя або подразнення шкіри після прийому алкогольних напоїв). В постмаркетинговий період спостерігались реакції на місці нанесення мазі, дерматит.
Пацієнти можуть мати підвищений ризик виникнення фолікулітів, акне та герпетичних вірусних інфекцій.
Нижче зазначено небажані реакції, спричинені застосуванням препарату. Частота виникнення побічних реакцій класифікується як:
- дуже часті (≥1/10),
- часті (≥1/100 до <1/10),
- рідкі (≥1/1000 до <1/100) та з невідомою частотою.
Небажані ефекти в межах кожної групи розміщені у порядку зменшення їх серйозності.
Таблиця 1
|
Клас системи органів |
Дуже часті ≥1/10 |
Часті ≥1/100, <1/10 |
Рідкі ≥1/1000, <1/100 |
Невідома частота (із доступних даних визначення частоти неможливе) |
|
Інфекційні та паразитарні захворювання |
|
Місцева інфекція шкіри, незалежно від етіології, що включає, але не обмежується такими інфекціями, як: герпетиформна екзема, фолікуліт, простий герпес, герпетична вірусна інфекція, варицеліформний пустульоз Капоші* |
|
Герпетична інфекція очей* |
|
Порушення з боку метаболізму та травлення |
|
Непереносимість алкоголю (почервоніння обличчя або подразнення шкіри після прийому алкогольних напоїв) |
|
|
|
Порушення з боку нервової системи |
|
Парестезія та дизестезія (гіперестезія, відчуття печіння) |
|
|
|
Порушення з боку шкіри та підшкірних тканин |
|
Свербіж |
Акне* |
Розацеа* Лентиго* |
|
Загальні розлади та порушення в місці введення |
Відчуття печіння та свербіж в місці нанесення |
Відчуття тепла, еритема, біль, подразнення, парестезія та висипання в місці нанесення |
|
Набряк у місці нанесення* |
|
Лабораторні та інструментальні дані |
|
|
|
Підвищений рівень препарату в крові* (див. розділ «Особливості застосування») |
* Про небажану реакцію повідомлено в постмаркетинговий період.
Профілактика виникнення загострень
В дослідженні профілактичного лікування (при застосуванні мазі двічі на тиждень) із залученням дорослих та дітей з середньою та тяжкою формами атопічного дерматиту відмічалось, що такі небажані реакції трапляються частіше, ніж у контрольній групі: імпетиго в місці нанесення (7,7 % дітей) та інфекції в місці нанесення (6,4 % дітей та 6,3 % дорослих).
Дослідження в постмаркетинговий період
Є інформація про випадки виникнення злоякісних новоутворень, включаючи шкірні (зокрема шкірна Т-клітинна лімфома) та інші види лімфом і рак шкіри у пацієнтів, які застосовували мазь такролімусу (див. розділ «Особливості застосування»).
Діти.
Частота, тип та тяжкість небажаних реакцій у дітей були подібними до реакцій у дорослих.
Повідомлення про можливі побічні реакції
Важливо повідомляти про можливі побічні реакції після реєстрації лікарського засобу. Це дає змогу проводити постійний моніторинг співвідношення користі та ризику лікарського засобу. Медичні працівники повинні повідомляти про будь-які підозрювані побічні реакції через національну систему повідомлень.
Термін придатності
3 роки.
Умови зберігання
Зберігати при температурі не вище 25 °С у недоступному для дітей місці.
Не застосовувати препарат після закінчення терміну придатності, зазначеного на упаковці.
Упаковка
0,03 % або 0,1 % мазь по 10 г, 30 г або 60 г в пластиковій тубі; по 1 тубі в картонній коробці.
Категорія відпуску з аптеки
За рецептом.
Відгуки користувачів
5.0 1 відгук
5 зірок 100% (1)
4 зірки 0% (0)
3 зірки 0% (0)
2 зірки 0% (0)
1 зірка 0% (0)
- МаринаХорошая мазь для избавления от детского дерматита, хотя и не дешевая, но она единственная нам помогла, спасибо.
Залишити відгук
Дивіться інші товари у категорії:
Крем для обличчя Caudalie Крем для обличчя з ботоксом Крем для депіляції обличчя Зарсіо Проліа екзодерил мазь ламізил мазь мікофін мазь пробіз нео сорб актив гель пробіз ціна зовіракс мазь актовегин мазь актовегін гель актовегін гель купити мазь актовегін ціна клотримазол мазь для жінок пімафуцин мазь клотримазол мазь для чоловиків флуконазол мазь ламізил мазь ціна екзифін мазь метрогіл гель для обличчя суфер ціна 1 ампула адреналін купити фітолізин мазь пенцикловір мазь мазь пенцикловір зовіракс мазь ціна ліпстер мазь према кідс троксерутин гель для обличчя троксевазинова мазь ліотрокс мазь мазь пімафуцин макмірор мазь актовегін мазь купити мазь актовегін лоратадин мазь свічки з папаверином тирозур гель від герпесу мазь вишневського ціна свічки з клотримазолом далацин гель ксеомин ціна перцева мазь уролесан пластинка ціна переднізолонова мазь налбуфін ціна купить налбуфін супрадин гель детралекс мазь свічки з іхтіолом стрепсілс з лідокаїном тіиотриазолін уколи ціна нутрілон преміум 1 мільгама мазь макмірор гель ніфедипін мазь купити корінь калгану меновазинова мазь ріопан гель живица мазь мазь лоратадин
Зверніть увагу
Інформація/інструкція до препарату носить ознайомчий характер і призначена виключно для інформаційних цілей.